原子や分子の量 - 物質の量を表すには
原子の構造を理解し、原子や分子の量を把握していきましょう。
原子の構造
原子とは、物質を構成する基本粒子のことです。
原子は正の電荷をもつ原子核と負の電荷をもつ電子から構成されています。さらに、原子核は正の電荷をもつ陽子と電荷をもたない中性子から構成されています。
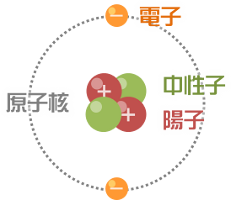
陽子もしくは電子の数を原子番号といい、陽子と中性子の数の合計を質量数といいます。
原子量
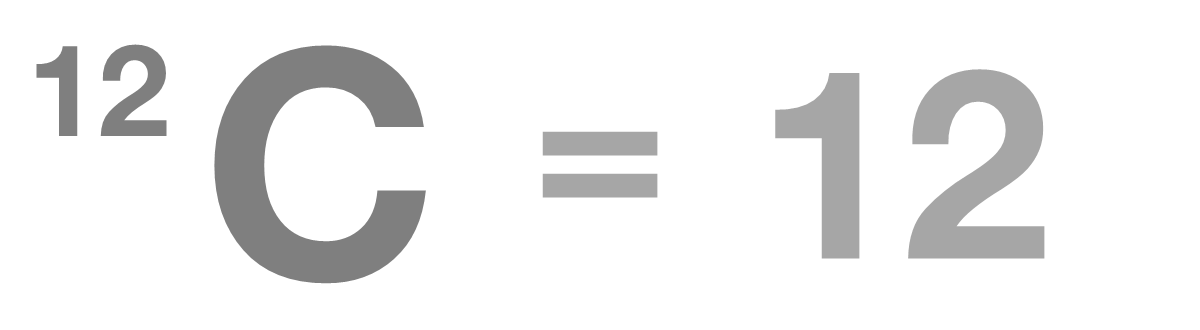
原子量(げんしりょう)とは、質量数12の炭素原子1個(12C)の質量を12とし、これと比較したときの原子の質量の比のことをいいます。相対原子質量(そうたいげんししつりょう)ともいいます。
比であるため単位はありません。
なぜ炭素が基準なのか
ここで、なぜ原子番号1の水素ではなく、原子番号12の炭素が基準となり原子量が定義されているのかと思うかもしれません。その理由は気体で捕集しにくい水素よりも、固体で手に入りやすい炭素が都合が良かったためです。
分子量
分子量(ぶんしりょう)とは、分子に含まれる元素の原子量の和のことです。相対分子質量(そうたいぶんししつりょう)ともいいます。
式量
イオン結晶は、結晶を構成する1ユニット単位を構成する原子を表す組成式で表現されます。組成式に含まれる原子の原子量の合計を式量(しきりょう)といいます。化学式量(かがくしきりょう)ともいいます。
スポンサーリンク
