化学平衡とル・シャトリエの原理

化学反応式において、ある反応『A + B ⇄ AB』が起こるとき、左辺から右辺へ進む反応『A + B → AB』を正反応(せいはんのう)、右辺から左辺へ進む反応『A + B ← AB』を逆反応(ぎゃくはんのう)といいます。
化学平衡の話に入る前にまず可逆反応と不可逆反応について見ていきましょう。
スポンサーリンク
可逆反応
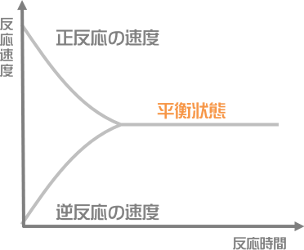
可逆反応(かぎゃくはんのう)とは、正反応、逆反応のどちらにも進行できる反応のことをいいます。正反応と逆反応の反応速度の差が、見かけ上の反応速度になります。

不可逆反応
不可逆反応(ふかぎゃくはんのう)とは、一方向にしか進まない(正反応しか起こらない)反応のことをいいます。

化学平衡
化学平衡(かがくへいこう)とは、可逆反応において正反応と逆反応の反応速度が等しくなり、見かけ上反応が終わったように見える状態のことをいいます。
スポンサーリンク
ル・シャトリエの原理(平衡移動の原理)
ル・シャトリエの原理(またはル・シャトリエの法則)とは、化学反応が平衡状態にあるとき、反応条件(濃度、圧力、温度)を変化させると、その変化を打ち消すように反応が進み、新たな平衡状態になるという法則のことです。
ル・シャトリエの原理には別名がいくつかあります。
ル・シャトリエ=ブラウンの原理、ル・シャトリエ=ブラウンの法則、平衡移動の原理(へいこういどうのげんり)、平衡移動の法則といわれることもあります。
次に、反応条件別に詳細を見ていきましょう。
濃度
ある成分の濃度を増加させると、その成分の濃度を減少させる方向に反応が進みます。逆に、ある成分の濃度を減少させると、その成分を増加させる方向に反応が進みます。
圧力
圧力を上げると、圧力を減らすため、気体の分子数が減少する方向に反応が進みます。逆に、圧力を下げると、圧力を上げるため、気体の分子数が増加する方向に反応が進みます。
温度
温度を上げると、温度を下げるため吸熱反応の方向へ反応が進みます。逆に、温度を下げると、温度を上げるため発熱反応の方向へ反応が進みます。
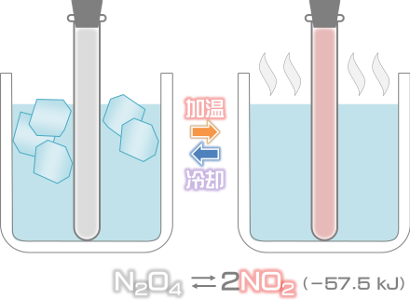
『N2O4(無色) ⇄ 2NO2(赤褐色)(- 57.2kJ)』の反応を例に見てみましょう。加温すると、加熱の影響を緩和する方向である吸熱反応の方向へ、反応が進みます。
N2O4 = 2NO2 - 57.2kJ
逆に、冷却すると冷却の影響を緩和する方向である発熱反応の方向へ、反応が進みます。
2NO2 = N2O4 + 57.2kJ
合格に役立つ参考書・問題集を確認しよう!
スポンサーリンク
