pH(水素イオン濃度指数)
pH(ピーエイチ、ペーハー)とは、水溶液の酸性、塩基性の度合いを表す0~14の数値のことです。
水素イオン濃度指数(すいそイオンのうどしすう)、水素イオン指数ともいいます。
pHは、水素イオン濃度の逆数の常用対数(じょうようたいすう)を用いて表されます。
pH = -log [H+] = log[H+]-
log(ログ)は、常用対数、すなわち、底が10の対数を表します。上の式の場合、[H+]-が10の何乗であるかを表しています。
[H+]は、水素イオン濃度のことで、水素イオンのモル濃度[mol/L]を表します。
pH = 7を中性とし、7以下を酸性、7以上をアルカリ性とします。
中和
中和(ちゅうわ)とは、酸と塩基が反応し、塩(えん)と水が生成する反応のことをいいます。
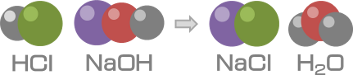
例えば、塩酸(HCl)に水酸化ナトリウム(NaOH)水溶液を加える中和反応では、水(H2O)と塩(えん)である塩化ナトリウム(NaCl)が生成します。ただし、塩化ナトリウムはナトリウムイオン(Na+)と塩化物イオン(Cl-)に電離しています。
HCl + NaOH → NaCl + H2O